|
|
Главная |
|
|
Пишите |
|
|
Ни одна вещь не возникает, не уничтожается, но каждая составляется из смешения существующих вещей или выделяется из них. (Анаксагор) |
Физическая химия занимается объяснением сущности химических явлений и установлением их общих закономерностей на основе физических (особенно микрофизических) принципов и экспериментальных данных.
Физическая химия включает квантовую химию, электрохимию, химическую термодинамику, химическую кинетику. Кроме того, в нее иногда включают коллоидную химию [раз так, то логично было бы включить нанохимию и химию суператомов, которые на сайте объединены в рамках нековалентной химии]. Так же здесь отдельно выделена химия атомов со сверхтяжелыми ядрами (химия сверхтяжелых атомов).
Основное различие между физической химией и химической физикой:
(Один из источников экспресс-обзоров на этой странице - Википедия).
Разделы страницы о физической химии:
Химия супрамолекулярная (или надмолекулярная, нековалентная) химия вынесена в независимый раздел (как органическая и неорганическая химия, которые также используют методы физической химии, но не входят в нее).
О свойствах отдельных атомов вы можете почитать, указав его в периодической таблице Менделеева.
Обзоры, порталы, новости...
Химическая кинетика изучает скорость химических реакций, её зависимость от внешних условий (температура, концентрации). Это один из важнейших разделов химии, показывающий какой именно продукт образуется в сложной системе. [Исследуется образование молекул на основе химической связи между атомами, т.е. как проходят химические реакции]
|
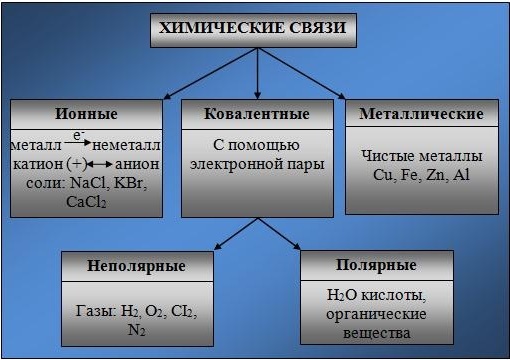
Химическая связь удерживает атомы или группы атомов друг около друга. Виды химической связи:
Ссылки:
|
Химические реакции - это процессы, протекающие в химическом веществе или в смесях различных веществ. При протекании химических реакций всегда образуются новые вещества. В сущности, это процесс изменения структуры молекулы. В результате реакции количество атомов в молекуле может увеличиваться (синтез), уменьшаться (разложение) или оставаться постоянным (изомеризация, перегруппировка). В ходе реакции изменяются связи между атомами и порядок размещения атомов в молекулах.
Химические реакции выявляют и характеризуют химические свойства данного вещества. Исходные вещества, взятые для проведения химической реакции, называются реагентами, а новые вещества, образующиеся в результате химической реакции, — продуктами реакции.
Химия изучает и описывает эти процессы как в макромасштабе (на уровне макроколичеств веществ), так и в микромасштабе (на атомно-молекулярном уровне). Внешние проявления химических процессов, протекающих в макромасштабе, нельзя непосредственно перенести на микроуровень взаимодействия веществ и однозначно их интерпретировать, однако такие переходы возможны при правильном использовании специальных химических законов, присущих только микрообласти (атомам, молекулам, ионам, взятым в единичных количествах).
Химическая термодинамика изучает процессы взаимодействия веществ методами термодинамики. Её главными направлениями являются:
Ссылки:
Растворами называются гомогенные системы, содержащие не менее двух веществ. Могут существовать растворы твердых, жидких и газообразных веществ в жидких растворителях, а также однородные смеси (растворы) твердых, жидких и газообразных веществ. Как правило, вещество, взятое в избытке и в том же агрегатном состоянии, что и сам раствор, принято считать растворителем, а компонент, взятый в недостатке - растворенным веществом. В зависимости от агрегатного состояния растворителя различают газообразные, жидкие и твердые растворы.
По соотношению преобладания числа частиц, переходящих в раствор или удаляющихся из раствора, различают растворы насыщенные, ненасыщенные и пересыщенные. Раствор, в котором данное вещество при данной температуре больше не растворяется, т.е. раствор, находящийся в равновесии с растворяемым веществом, называют насыщенным, а раствор, в котором еще можно растворить добавочное количество данного вещества, - ненасыщенным.
По относительным количествам растворенного вещества и растворителя растворы подразделяют на разбавленные и концентрированные. Сравнивая растворимость различных веществ, видно, что насыщенные растворы малорастворимых веществ являются разбавленными, а хорошо растворимых веществ - хотя и ненасыщенные, но довольно концентрированными.
В зависимости от того, электронейтральными или заряженными частицами являются компоненты раствора, их подразделяют на молекулярные (растворы неэлектролитов) и ионные (растворы электролитов). Одна из характерных особенностей растворов электролитов заключается в том, что они проводят электрический ток.
В 1840 году Герман Иванович Гесс сформулировал фундаментальный закон термохимии – закон постоянства количества теплоты: "Каким бы путём не совершалось соединение, – имело ли оно место непосредственно или происходило косвенным путём в несколько приёмов, – количество выделившейся при его образовании теплоты всегда постоянно".
В 60-е годы XIX века независимо друг от друга два выдающихся исследователя – Пьер Эжен Марселен Бертло и Ханс Петер Юрген Юлиус Томсен высказали предположение о том, что тепловой эффект реакции является мерой химического сродства между реагентами. Основное положение данного подхода Бертло сформулировал следующим образом: "Теплота, выделяющаяся при реакции, служит мерой суммы физических и химических работ, совершаемых при этой реакции. …Принцип максимальной работы заключается в том, что всякое <самопроизвольное> химическое превращение… стремится к образованию тела или системы тел, которые выделяют наибольшее количество тепла".
В середине XIX века появились экспериментальные данные, возродившие интерес к идеям Бертолле, в частности, к введённому им понятию химической массы, которое, по мнению Бертолле, определяет протекание реакции и состав её продуктов. В 1850 г. Александер Уильям Уильямсон, исследуя сложные эфиры, установил, что реакции этерификации являются обратимыми и приводят к наступлению динамического равновесия, в котором присутствуют и исходные вещества, и продукты реакции. Немецкие химики Генрих Розе и Роберт Вильгельм Бунзен в 1851-1853 гг. показали, что реакции обмена часто являются обратимыми и направление реакции можно изменить путём подбора соответствующих условий её протекания. В 1874-1878 гг. американский физик Джозайя Уиллард Гиббс опубликовал работы по теоретическому рассмотрению термодинамики химического равновесия; Гиббс ввёл в термодинамику понятия свободной энергии, термодинамического и химического потенциалов.
Огромный вклад в изучение состояния химического равновесия внёс Якоб Генрик Вант-Гофф, опубликовавший в 1884 г. фундаментальную работу
"Этюды химической динамики", в которой, связав представления о химическом равновесии с двумя началами термодинамики,
рассмотрел влияние температуры на химическое равновесие. Вант-Гофф вывел формулу изохоры химической реакции:
dlnK/dT = Q/RT2 (Изохора Вант-Гоффа), где К – константа равновесия, Q – теплота реакции.
Вант-Гофф сформулировал также принцип подвижного равновесия и показал, что он выполняется для любых типов равновесных систем:
"Каждое равновесие… при понижении температуры смещается в сторону той системы, при образовании которой выделяется теплота".
В 1885 г. он термодинамически вывел закон действующих масс Гульдберга-Вааге.
Вывод уравнения изотермы химической реакции, связывающего константу равновесия с термодинамическими потенциалами
осуществил в 1886 г. французский физик Пьер Дюгем.
Звукохимия (сонохимия) исследует звукохимическим реакции - химические реакции, возникающих под действием мощных акустических колебаний. К области звукохимии так же относятся некоторые физико-химические процессы и эффекты в звуковом поле: сонолюминесценция, диспергирование вещества при действии звука, эмульгирование и другие коллоидно-химические процессы. Звукохимия изучает и процессы кавитации.
Обычно звукохимические процессы исследуют в ультразвуковом диапазоне (от 20 кГц до нескольких МГц). Звуковые колебания в килогерцовом диапазоне и инфразвуковой диапазон изучаются значительно реже.
Электрохимия изучает химические процессы в веществах и межфазовых границах при протекании через них электрического тока, Исследуются процессы окисления-восстановления, перенос ионов и электронов в проводниках. Перенос заряда с молекулы на молекулу в электрохимии не рассматривается.
Имеет теоретический и прикладной разделы. Теоретическая электрохимия занимается теорией электролитов и электрохимией гетерогенных систем.
Структурная химия (стереохимия) — раздел, область химии, изучающая связь различных физических и физико-химических свойств различных веществ с их химическим строением и реакционной способностью. Структурная химия рассматривает не только геометрическое строение молекул; изучаются также: 1) длины химических связей, 2) валентные углы, 3) координационные числа, 4) конформации и конфигурации молекул; 5) эффекты их взаимного влияния, 6) ароматичность.
Особенности пространственного строения обнаруживаются в появлении стереоизомеров. Эти особенности влияют на скорость и направление химических превращений, на физические свойства веществ, на характер их физиологического действия и др. (Из Википедии)
Проще говоря, структурная химия - прикладная междисциплинарная наука, изучающая различными методами структуру молекул вещества.
Стереохимические методы анализа чрезвычайно важны в фармацевтике, т.к. молекулы одного состава, но зеркально несимметричные (хиральные) могут не только быть бесполезными но даже губительно вредными лекарствами.
Коллоидная химия (др.-греч. kolla — клей) — физическая химия дисперсных систем и поверхностных явлений, возникающих на границе раздела фаз. [Не логичнее ли было это отнести к молекулярной физике?] Изучает адгезию, адсорбцию, смачивание, коагуляцию, электрофорез. Разрабатывает технологии строительных материалов, бурения горных пород, зол-гель технологии. Играет фундаментальную роль в нанотехнологии.
Возможно, эту дисциплину стоит включить в супрамолекулярную химию.
Суператомы - молекулы из атомов одного химического элемента, ведущие себя как псевдоатом дугого элемента. Например, несколько "слипшихся" атомов алюминия могут в химических реакциях вести себя аналогично атому йода [!].
Здесь приводятся сведения о химических свойствах атомов со сверхтяжелыми ядрами.
Квантовая химия рассматривает строение и свойства химических соединений, реакционную способность, скорость и механизм химических реакций на основе квантовой механики. Ее предметами являются:
Ссылки:
Химия высоких энергий (ХВЭ) изучает химические реакции и превращения, происходящие в веществе под воздействием нетепловой энергии: ионизирующего излучения, света, плазмы, ультразвука, механических ударов и др. В сответствии с этими энергетическими агентами ХВЭ состоит из следующих основных разделов:
Ключевые слова для поиска сведений о физической химии:
На русском языке: физическая химия, кинетика и термодинамика химических реакций, квантовая теория химических связей,
сонохимия, звукохимия, нанохимия, электрохимия, фотохимия, радиохимия, термохимия,
химия коллоидов, химия суператомов, квантовая химия, химия сверхтяжелых атомов,
холодный ядерный синтез, современная алхимия, нетермоядерное превращение элементов, эмулоны, структура воды;
На английском языке: physical chemistry, alchemy, cold fusion.
|
|
|